太阳成集团2018年大学生生物化学实验技能大赛初赛试题及答案
一、选择题
1.在容量瓶使用方法中,下列操作不正确的是()
A.使用容量瓶前检查它是否漏水
B.容量瓶用蒸馏水洗净后,不再用碱液润洗
C.将氢氧化钠固体放在天平托盘的滤纸上,准确称量并放入烧杯中溶解后,立即注入容量瓶中
D.定容后塞好瓶塞,用食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶倒转摇匀
2.下列操作中,哪个是容量瓶不具备的功能()
A.直接法配制一定体积准确浓度的标准溶液
B.定容操作
C.测量容量瓶规格以下的任意体积液体
D.准确稀释某一浓度的溶液
3.将固体溶质在小烧杯中溶解,必要时可加热,溶解后溶液转移到容量瓶中时,下列操作错误的是()
A.趁热转移
B.使玻璃棒下端和容量瓶颈内壁相接触,但不能和瓶口接触
C.缓缓使溶液沿玻璃和颈内壁全部注入容量瓶内
D.用洗瓶小心冲洗玻璃和烧杯内壁3-5次,并将洗涤液一并移至容量瓶内
4.使用容量瓶时,下列哪个操作是正确的()
A.将固体试剂放入容量瓶中,加入适量的水,加热溶解后稀释到刻度
B.热溶液应冷至室温后再移入容量瓶稀释至标线
C.容量瓶中长久贮存溶液
D.闲置不用时,盖紧瓶塞,放在指定的位置
5.容量瓶上标有:①温度②浓度③容量④压强⑤刻度线⑥酸式或碱式 这六项
A.①③⑤B.③⑤⑥C.①②④D.②④⑥
6.有关容量瓶的说法,正确的是()
A.容量瓶是一种容积精确的仪器B.容量瓶不宜长期存放溶液
C.容量瓶可以用作反应容器D.容量瓶可用来直接溶解固体溶质
7.用15ml的移液管移出的溶液体积应记为()
A.15mL B. 15.0mL C. 15.00mL D. 15.000mL
8.欲配制1000毫升0.1.mol/L的NaOH溶液,需要称取NaOH(M[NaOH]=40g/mol)( )
A. 40g B. 4g C. 0.4g D. 0.04g
9.量取甲醇10.0mL,应选取以下哪种量器()
A.量筒 B.烧杯C.刻度吸管D.移液管
10.配制好的NaOH需贮存于()中
A.棕色橡皮塞试剂瓶B.白色橡皮塞试剂瓶
C.白色磨口塞试剂瓶D.塑料瓶
11.如果发现容量瓶漏水,则应()
A调换磨口塞B在瓶塞周围涂油C停止使用D摇匀时勿倒置
12.使用移液管时,应将其下口插入液面以下( )
A. 0.5-1cmB. 5-6cm C. 1-2cm D. 7-8cm
13.欲量取9ml HCl配制标准溶液,选用的量器是()
A.吸量管 B.滴定管 C.移液管 D.量筒
14.配制好的盐酸溶液贮存于()中
A棕色橡皮塞试剂瓶B白色橡皮塞试剂瓶C白色磨口试剂瓶D试剂瓶
15.配制一定物质的量浓度的某溶液,下列情况,会使配置结果偏高的是()
A.未冷却即转移、定容
B.未洗涤烧杯和玻璃棒
C.定容时仰视刻度线观察页面
D.容量瓶中原来含有少量蒸馏水
16.滴定分析法主要适合于()
A.微量分析法B.痕量分析法C.微量成分分析D.常量成分分析
17.某基准物A的摩尔质量为500 g/moL,用于标定0.1mol/L的B溶液,设反应为A+2B=P,则每份基准物的称取量宜为()克?
A. 0.1-0.2 B. 0.4-0.7 C. 0.7-1.0 D. 1.0-1.5
18.下列物质中,可以用直接法配制标准溶液的是()
A.固体NaOH B.浓HCl C.固体K2Cr2O7D.固体Na2S2O3
19.用0.1000mol/L NaOH标准溶液滴定0.1mol/L HAc溶液时,合适的指示剂是( )
A.酚酞B.甲基红C.甲基橙D.溴百里酚蓝
20.配位滴定法测定Al3+的含量(不含其它杂质离子),最常用的简便方法是()
A.直接滴定法B.间接滴定法C.返滴定法D.置换滴定法
21.配位滴定中,若Kf'(MIn)> Kf'(MY),会出现( )
A.指示剂的封闭现象B.指示剂的僵化现象
C.指示剂的氧化变质现象D.终点提前现象
22.以CaCO3为基准物质标定EDTA溶液的实验中,需要EDTA溶液荡洗2-3次的仪器是( )
A.滴定管B.容量瓶C.移液管D.锥形瓶
23.用EDTA测定水中的Ca2+的含量时,Mg2+有干扰,实验中采用何种方法消除其干扰()
A.加三乙醇胺B.调节pH值≈12 C.加KCN D.分离
24.用KMnO4滴定Fe2+时,酸性介质宜由()提供
A. HCl B. HNO3C. HAc D. H2SO4
25.在滴定分析中,若要准确移取0.1000 mol/L硼砂溶液25.00mL,则应选用的器皿是( )
A.滴定管B.容量瓶C.移液管D.量筒
26.在EDTA配合滴定中,只考虑酸度影响,下列叙述正确的是()
A.酸效应系数越大,配合物的稳定性越大
B.酸效应系数越小,配合物的稳定性越大
C. pH越大,酸效应系数越大
D.酸效应系数越大,滴定突跃范围越大
27.将双指示剂法用于未知碱液的定性分析,若V1为酚酞指示剂变色消耗HCl的体积,V2为甲基橙指示剂变色消耗HCl的体积。当V1> V2时,未知碱液的组成是( )
A. NaOH B. NaHCO3C. Na2CO3,NaOH D. Na2CO3,NaHCO3
28.实验室标定KMnO4溶液,常用的基准物质是()
A. Na2CO3B. Na2S2O3C. Na2C2O4D. K2Cr2O7
选择题答案:
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
13 |
14 |
C |
C |
A |
B |
A |
A |
C |
B |
C |
D |
C |
C |
C |
C |
15 |
16 |
17 |
18 |
19 |
20 |
21 |
22 |
23 |
24 |
25 |
26 |
27 |
28 |
C |
D |
B |
C |
A |
C |
A |
A |
B |
D |
C |
B |
C |
C |
二、判断题
1.各种电源是否有电,可用试电笔检验。(错误)
2.实验室禁止私拉乱接电线,实验过程中自制非标设备时,应报请实验室管理人员批准,然后请电气专业人员按照标准安全的连接。(正确)
3.在充满可燃气体的环境中,可以使用手动电动工具。(错误)
4.在易燃、易爆、易灼烧及有静电发生的场所,可以使用化纤防护用品。(错误)
5.连接在接线板上的用电总负荷不能超过接线板的最大容量。(正确)
6.身边有人严重触电,应当首先切断电源,然后进行紧急抢救如人工呼吸,并立即拨打急救电话120。(正确)
7.化学泡沫灭火器可扑救一般油质品、油脂等的火灾,但不能扑救醇、酯、醚、酮等引起的火灾和带电设备的火灾。(正确)
8.开启氨水、浓盐酸瓶应该在通风櫉中进行。(正确)
9.能相互反应产生有毒气体的废液,不得倒入同一收集桶中。若某种废液倒入收集桶会发生危险,则应单独暂存于一容器中,并贴上标签。(正确)
10.汞及其化合物、砷及其无机化合物、黄磷、碘甲烷、甲基丙烯酸甲酯、氰化物等具有剧毒性。(正确)
11.气体钢瓶使用后,可以不关闭阀门。(错误)
12.过氧化物、高氯酸盐、叠氮铅、乙炔铜、三硝基甲苯等属于易爆物质,受震或受热可发生热爆炸。(正确)
13.对固态酸、碱可用手直接操作。(错误)
14.创伤伤口内有玻璃碎片等大块异物时,应在去医院救治前尽快取出。(正确)
15.危险化学品用完后就可以将安全标签撕下。(错误)
16.Hg通常经过皮肤和消化道进入人体。(错误)
17.禁止穿拖鞋、背心、短裤(裙)进入实验室,高跟鞋可以进实验室。(错误)
18.丙酮、氢氧化钠、氨等具有低毒性。(正确)
19.打开氨水、硝酸、盐酸等药品瓶封口时,应先盖上湿布,用冷水冷却后再开瓶塞,以防溅出,尤其在夏天更应注意。(正确)
20.HCN进入机体,抑制呼吸酶作用,造成细胞内窒息,从而引起组织中毒性缺氧,全身性中毒症状。(正确)
21.实验室毒物进入人体有三条途径即皮肤、消化道和呼吸道。实验室防毒应加强个人防护。(正确)
22.对剧毒品采取必要的保安措施,防止剧毒化学品被盗、丢失或者误售、误用;发现剧毒化学品被盗、丢失或者误售、误用时,必须立即向当地公安部门报告。(正确)
23.实验过程中应尽量避免实验仪器在夜间无人看管的情况下连续运转,如果必须在夜间使用,应严格检查实验仪器的漏电保护装置及空气开关等工作正常。(正确)
24.火灾发生后,受到火势威胁时,要当机立断披上浸湿的衣物,被褥等向安全出口方向冲去。(正确)
25.扑救毒害性、腐蚀性或燃烧产物毒害性较强的火灾时,必须配戴防护面目。(正确)
26.如果可燃液体在容器内燃烧时,应从容器的一侧上部向容器中喷射但喷射但注意不能将喷流直接喷射在燃烧液面上,防止灭火剂的冲力将可燃液体冲出容器而扩大火势。(正确)
27.碱灼伤时,必须先用大量流水冲洗至皂样物质消失,然后可用1%-2%醋酸或3%硼酸溶液进一步冲洗。(正确)
28.因为实验需要,可以在实验室存放大量气体钢瓶。(错误)
29.水具有导电性,不宜扑救带电设备的火灾,不能扑救遇水燃烧物质或非水溶性燃烧液体的火灾。(正确)
30.使用手提灭火器时,拔掉保险销,对准着火点根部用力压下压把,灭火剂喷出,就可灭火。(正确)
31.液体着火时,应用灭火器灭火,不能用水扑救或其他物品扑打。(正确)
32.隔离灭火法是将可燃物与引火源或氧气隔离开来,可防止火势继续扩大。(正确)
33.如酚灼伤皮肤,先用浸了甘油或聚乙二醇和酒精混合液(7:3)的棉花除去污物,再用清水冲洗干净,然后用饱和硫酸钠溶液湿敷。但不可用水直接冲洗污物,否则有可能使创伤加重。(正确)
34.将醇液直接加入到室温以下的硫酸-硝酸的混酸中不会引起爆炸,而加入到未冷却的硫酸-硝酸的混酸中会引起爆炸。(错误)
35.常用的化学试剂如:苯、乙醚、甲苯、汽油、丙酮、甲醇和煤油均属于易燃物质。(正确)
36.在使用化学品的工作场所吸烟,可能会造成火灾和爆炸,但不会中毒。(错误)
37.用泡沫灭火剂扑灭油罐火灾时,如果火势很大,有时并不能将火完全扑灭,会发生闷燃引起爆炸。(正确)
38.有毒化学品在水中的溶解度越大,其危险性越大。(正确)
39.使用离心机时,当部分装载时,离心管可随意放在转头中而不用考虑平衡。(错误)
40.离心过程中,若听到离心机有异常响声,待离心完成后再停机检查原因。(错误)
三、简答题
1.什么情况下采用减量法称量法,如使用电子天平具体如何操作?
答:用于称取易吸湿、易氧化、易与二氧化碳反应的物质。先用电子天平称取盛有试样的带盖称量瓶重量,记录数据后,取出称量瓶,打开瓶盖,轻轻敲动瓶口上方,将试样抖落入接受试样的容器上方。盖好称量瓶盖后,再次称取称量瓶重量,两次数据之差为所取试剂质量。
2.易挥发的液体样品,如称取浓HCl试样时,可采用什么方法,如何操作?
答:可采用增量法。称取浓HCl时,可先在100mL具塞锥形瓶中加适量水,准确称量后,加入适量试样,立即盖上瓶盖再次称量。
3.三级分析天平可称准至±0.0001g,要使称量误差不大于0.1%,至少应称取多少试样?
答:因为每称一份试样需称量两次,所以称一份试样的绝对误差为+0.0002g,因此至少应称取+0.0002g/0.1%=0.2g。
4.配置0.1mol/L的盐酸标准溶液10L,所用盐酸质量百分含量为37%,密度1.19g/mL,理论上所需体积为多少毫升?
答:设所需体积为Vml,利用盐酸物质量守恒原理,有等式:
10L×0.1mol/L=Vml×1.19×37%÷36.5 V=82.9mL
5.简述移液管使用的要求及注意事项。
答:1)移液管(吸量管)不应在烘箱中烘干。2)移液管(吸量管)不能移取太热或太冷的溶液。3)同一实验中应尽可能使用同一支移液管。4)移液管使用完毕后,应立即用自来水及蒸馏水冲洗干净,置于移液管架上。5)移液管和容量瓶常配合使用,因此在使用前常作两者的相对体积校准。6)在使用吸量管时,为了减少测量误差,每次都应从最上面刻度(0刻度)处为起始点,放出所需体积的溶液,而不是需要多少体积就吸取多少体积。
6.简述容量瓶的使用步骤。
答:1)使用前检查瓶塞处是否漏水。2)把准确称量好的固体溶质放在烧杯中,用少量溶剂溶解。然后把溶液转移到容量瓶里。为保证溶质能全部转移到容量瓶中,要用溶剂多次洗涤烧杯,并把洗涤溶液全部转移到容量瓶里。转移时要用玻璃棒引流。3)向容量瓶内加入的液体液面离标线1厘米左右时,应改用滴管小心滴加,最后使液体的弯月面与标线正好相切。若加水超过刻度线,则需重新配制。4)盖紧瓶塞,用倒转和摇动的方法使瓶内的液体混合均匀。
7. NaOH的标准溶液如吸收了空气中的CO2,用它测定某强酸浓度,分别用甲基橙或酚酞作指示剂,对测定结果的准确度有何影响?
答:不相同。NaOH吸收空气中CO2生成Na2CO3,以甲基橙为指示剂时,滴定终点时,NaOH和Na2CO3皆转化为NaCl,对HCl溶液消耗无影响,不影响分析结果。以酚酞为指示剂滴定到终点时,Na2CO3只转化为NaHCO3,消耗HCl溶液的体积减少,故标定HCl溶液的浓度偏高。
8.滴定至临近终点时加入半滴的操作是怎样进行的?
答:加入半滴的操作是:将酸式滴定管的旋塞稍稍转动或碱式滴定管的乳胶管稍微松动,使半滴溶液悬于管口,将锥形瓶内壁与管口接触,使液滴流出,并用洗瓶以纯水冲下。
9.用Na2C2O4标定KMnO4时候,为什么必须在H2SO4介质中进行?酸度过高或过低有何影响?可以用HNO3或HCl调节酸度吗?为什么要加热到70~80℃?溶液温度过高或过低有何影响?
答:若用HCl调酸度,Cl-具有还原性,与KMnO4作用。若用HNO3调酸度,HNO3具有氧化性。故只能在H2SO4介质中进行。滴定在强酸性溶液中进行,酸度过低,KMnO4与被滴定物作用生成MnO(OH)2沉淀,反应不能按一定的计量关系进行。室温下,KMnO4与Na2C2O4的反应速度慢,须将溶液加热到70~80℃,但温度不能超过90℃,否则Na2C2O4分解。
10.请画出回流提取装置的示意图,并简述其操作要点。
答:回流提取装置如图所示:
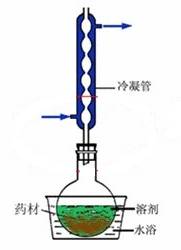
操作要点:①装置的安装顺序;由下至上。②冷凝水的方向:下进上出。③打开顺序:先开冷凝水,后打开加热装置。④装料量:烧瓶体积的二分之一至三分之一。⑤防止暴沸。
11.请画出连续回流提取装置(索氏提取)的示意图,并简述其操作要点。
答:连续回流提取装置如图所示:
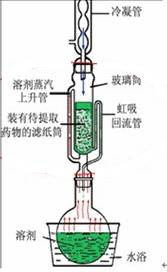
操作要点:①各个部分的干燥。②装置的搭建:类似于回流提取。③被提取物的放置:滤纸包好,注意不要漏。④加入提取溶剂:溶剂量应能够保证虹吸发生。⑤索氏提取器、烧瓶及冷凝管均要固定。
12.请列举常用的液固分离方法及其适用范围。
答:①离心分离:可分为过滤式分离,适合颗粒比较大的物理;沉降式离心,适合颗粒较小的分类。②过滤分离:利用不同过滤介质的孔径大小进行分离,可使用抽滤、膜分离等。
13.请画出抽滤时所使用的装置,并简述其操作要点。
答:抽滤装置如图所示:
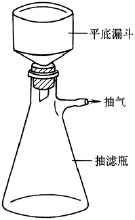
操作要点:①注意布氏漏斗下端与抽气口的相对位置。②抽滤时应使用两张滤纸,并注意滤纸大小与漏斗口径应吻合。③抽滤前应润湿滤纸,并检漏。④关闭时应先拔掉抽气管,再关闭真空泵。⑤转移滤液时,应防止滤液从抽气口泄露。
14.请列举实验室常用的粉碎设备,并简述其操作要点。
答:①小型粉碎机:检查物料中是否含有金属性杂物;粉碎时间不易过长(产热),含糖较多或湿物料不宜采用。②高速匀浆机:适合对新鲜物料及动物组织的破碎,注意清洗。③超声波细胞破碎仪:注意超声功率,长时间容易产热。④研钵:适合少量物料的粉碎,有时需加助研剂。
15.试简述旋转蒸发仪的操作原理。
答:通过电子控制,使烧瓶在最适合速度下,恒速旋转以增大蒸发面积。通过真空泵使蒸发烧瓶处于负压状态。蒸发烧瓶在旋转同时置于水浴锅中恒温加热,瓶内溶液在负压下在旋转烧瓶内进行加热扩散蒸发。
16.紫外-可见分光光度法测定药物含量时,溶剂如何选择?波长如何选择?
答:对溶剂的要求:①对含量测定无干扰,如含有杂原子的有机溶剂,常常含有较强的末端吸收,因此在使用时,它们的使用范围均不能小于截止使用波长。所以,在测定供试品之前,先对溶剂的吸光度进行测定,220-240nm范围内不得过0.40,在241~250nm范围内,不得过0.20,在251~300nm之间不得过0.10,在300nm以上不得过0.05nm;②注意溶剂的挥发性,在选用时尽量避免溶剂挥发带来的影响;③注意溶液的pH值稳定,在测定时如果必须要求一定pH,则尽量选用缓冲盐调节pH,以保证pH的稳定性。
对波长的选择:①进行供试品和对照品的全波长扫描,要以该物质的最大吸收波长为检测波长进行含量测定;②该检测波长不能与其他物质或溶剂产生交叉干扰。
17.简述721型(尤尼柯UV-2000型)紫外-可见分光光度仪的使用规程。
答:①接通电源、打开仪器开关,打开暗箱盖,预热20~30min;②通过“λ”旋钮,选定所需波长;③将参比液装入比色皿,放入比色架中,盖上暗盒盖,此时光路开启,让参比溶液置于光路上,调节透光率或吸光度按钮,调到透光率100%或吸光度0;④利用拉杆将待测液推入光路,读取吸光度值(或相应T值),读取后将暗盒盖打开;⑤每当改变波长测量时,必须重新调零、调满;⑥仪器使用完毕,取出比色皿,洗净、晾干,关闭电源开关,拔下电源插头,然后罩好防尘护罩,复原仪器。⑦清理实验材料,填写使用记录,打扫实验室。
18.紫外-可见分光光度仪进行含量测定时,如何绘制标准曲线?
答:①称取对照品适量,按比例稀释,配制好各种浓度的稀释液;②调试紫外分光光度仪,设定最大吸收波长,参比溶液校正;③将供试液放入吸收池,进行测定,记录读数;④以浓度为横坐标,吸光度为纵坐标,利用excel或者其他软件,计算得到回归方程,求得r值,要求r值达到0.999以上。
19.简述薄层色谱法的一般程序有哪些?并简要说明各步骤的注意事项。
答:薄层色谱法一般需要:制板、点样、展开、显色4大步骤。
(1)制板:①硅胶类型的选择,如硅胶G、硅胶H、硅胶GF254等;②硅胶与粘合剂的配比为1:3,有时还需要用0.2%~0.5%的CMC-Na溶液;③活化时,一定要等自然晾干后,再放入105℃烘箱20~30min。
(2)点样:①点样量2~5μL;②点样时要尽量控制点的大小,在3mm以下;③点样间距一般要大于8mm;④点样的基线与玻璃下沿要有1cm~1.5cm的距离。
(3)展开:①展开剂一定要配精确,混合好后,加入到展开槽中;②加入展开剂后要饱和20~30min,必要时,将薄层板也放入双槽层析缸中共同饱和,以控制边缘效应;③注意控制溶剂前沿,不要展开太过;④计算Rf值,控制在0.2~0.8之间。
(4)显色:①本身有颜色的,日光下检识即可;②需要喷显色剂的,可以显色后检识;③有荧光的,可以在254nm或365nm下进行检识。
20.以硅胶为填料,试述湿法装柱和干法装柱、加样及洗脱的步骤要点。
答:湿法装柱:①先把硅胶用适当的溶剂拌匀后,除去气泡,并滤掉大颗粒或杂质;②将混合溶液沿层析柱的内壁缓慢倒入(层析柱下端垫有棉花或碎瓷片),并不断敲打柱子两侧,以使硅胶均匀无气泡;③上端缓慢加入淋洗剂,保证柱子上端液面不干涸,进行冲洗(避免上层硅胶被冲起);④用双连球或者加压装置,对层析柱进行加压,以提高柱效。
干法装柱:①柱子里直接填入硅胶;②轻轻敲打柱子两侧,至硅胶界面不再下降为止;③然后再填入硅胶至合适高度,最后再用油泵直接抽,使柱子装的比较结实;④用淋洗剂“走柱子”,上面加压,下面再用油泵抽,增加柱效。






